如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
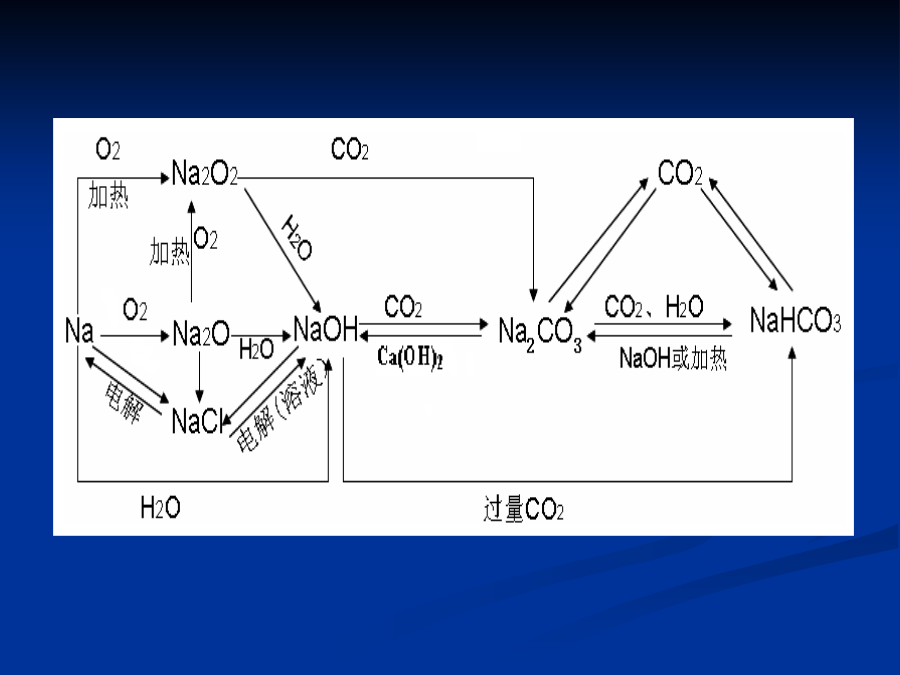
钠及碱金属(1)Na2O2的强氧化性①Na2O2与SO2反应:Na2O2+SO2===Na2SO4。②Na2O2投入FeCl2溶液中,可将Fe2+氧化成Fe3+,同时生成Fe(OH)3沉淀。③Na2O2投入氢硫酸中,可将H2S氧化成单质硫,溶液变浑浊。④Na2O2投入Na2SO3溶液,可将SO32-氧化成SO42-。⑤Na2O2具有漂白性,投入品红溶液中,可使品红溶液褪色。(2)有关Na2O2与CO2、H2O的反应①电子转移关系当Na2O2与CO2、H2O反应时:2Na2O2~O2~2e-。②固体质量关系当Na2O2与CO2、H2O反应时,相当于固体(Na2O2)只吸收了CO2中的“CO”或H2O中的“H2”;可以看作发生相应的反应:Na2O2+CO===Na2CO3、Na2O2+H2===2NaOH(实际上两反应不能发生)。③先后顺序关系一定量的Na2O2与一定量的CO2和H2O的混合物的反应,可看作Na2O2先与CO2反应,待CO2反应完全后,Na2O2再与H2O发生反应。[变式训练]1.(2008·北京理综)1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是()A.Na2CO3B.Na2O2Na2CO3C.NaOHNa2CO3D.Na2O2NaOHNa2CO3【自我检测】1.用一团脱脂棉包住少量Na2O2粉末,滴入几滴水,棉花燃烧,是因为Na2O2和H2O反应生成________,并且反应放________。2.用一团脱脂棉包住少量Na2O2粉末,用嘴和玻璃管向棉花上吹气,棉花燃烧,是因为________________反应生成O2并且反应放热。3.为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是()①Na2O2中阴、阳离子的个数比是1∶1②Na2O2分别与水及CO2反应产生相同量氧气时,需水和CO2的质量相等③Na2O2分别与水及CO2反应产生相同量氧气时,转移电子的物质的量相等④Na2O2的漂白原理与SO2的漂白原理相同⑤Na2O2与SO2反应生成Na2SO3与H2O⑥Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物⑦Na2O2与水反应,Na2O2既是氧化剂,又是还原剂⑧Na2O2投入到紫色石蕊试液中,溶液先变蓝,后褪色A.①③⑥⑧B.③⑦⑧C.②⑤⑥⑦D.①④⑧(1)与足量酸反应的比较①反应速率浓度相同时,NaHCO3比Na2CO3与酸反应速率大。②耗酸量a.等物质的量的Na2CO3、NaHCO3与酸反应时,消耗酸的物质的量之比为2∶1。b.等质量时Na2CO3、NaHCO3消耗酸的物质的量之比为84∶53。③生成CO2的量a.等物质的量的Na2CO3、NaHCO3产生的CO2一样多。b.等质量时NaHCO3比Na2CO3产生的CO2多。(2)Na2CO3、NaHCO3的鉴别(3)Na2CO3与NaHCO3的相互转化【自我检测】1.向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再生成CO2为止,则在此过程中,溶液中碳酸氢根浓度先逐渐________,而后________,其对应的离子方程式为:_____________,_____________。增大减少CO32-+H+===HCO3-HCO3-+H+===CO2↑+H2O2.除去NaHCO3溶液中少量Na2CO3的方法是___________。除去Na2CO3粉末中NaHCO3的方法是________。向溶液通足量CO2加热3、(2010·上海)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是()[变式训练]2.一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图。下列有关叙述正确的是()A.通入的CO2气体在标准状况下可能大于22.4LB.A溶液中n(NaOH)=2n(Na2CO3)C.A溶液中既含Na2CO3,又有NaHCO3D.A溶液中一定只有Na2CO31.(2010·安徽)将0.01mol下列物质分别加入100mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)()①Na2O2②Na2O③Na2CO3④NaClA.①>②>③>④B.①>②>④>③C.①=②>③>④D.①=②>③=④解析:四种物质溶于水后所得溶液中溶质分别是①0.02molNaOH,②0.02molNaOH,③0.01m