如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
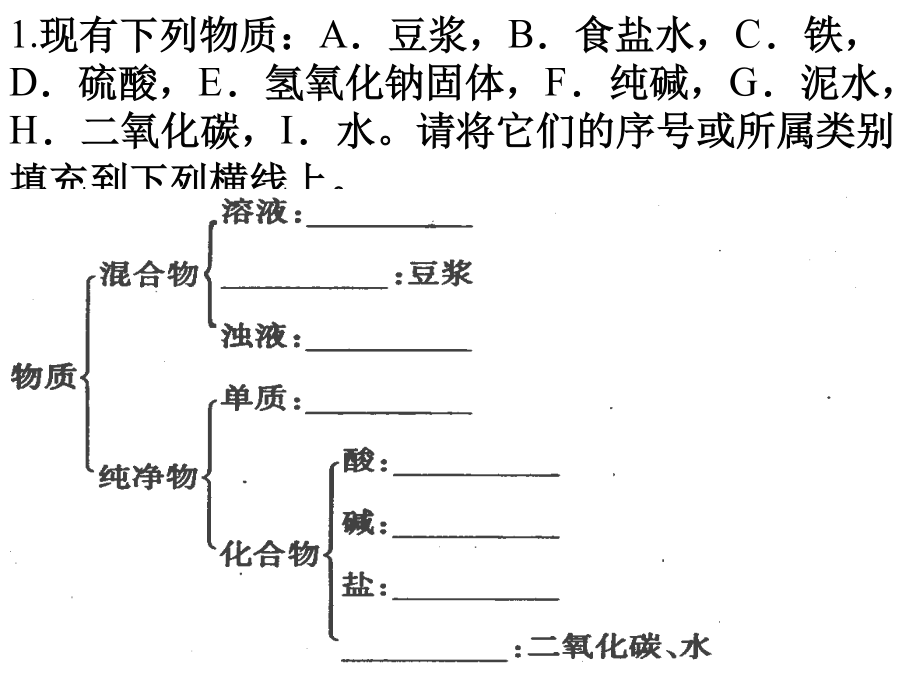
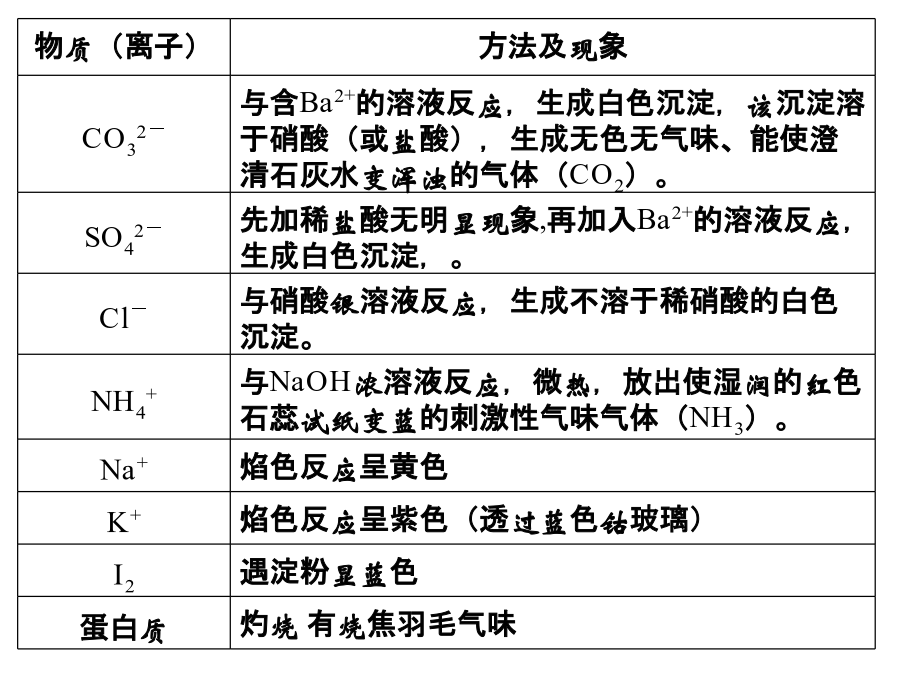
氯气的工业制法:漂白粉的生产原理:物质1.现有下列物质:A.豆浆,B.食盐水,C.铁,D.硫酸,E.氢氧化钠固体,F.纯碱,G.泥水,H.二氧化碳,I.水。请将它们的序号或所属类别填充到下列横线上。2.设NA表示阿伏加德罗常数的值,下列说法中正确的是()A.17gOH-与19gH3O+所含电子数相等B.10克氖气所含原子数约为6.02×1023C.标准状况下,11.2LH2O与常温常压下8.5gNH3所含分子数相等D.常温常压下,32gO2和O3的混合气体所含原子数为2NA分离提纯方法_____mL容量瓶、烧杯、玻棒、胶头滴管、量筒、托盘天平及砝码、药匙第二课时4.下列仪器常用于物质分离的是①②③④⑤⑥A.①③⑤B.②③⑤C.②④⑤D.①②⑥5、如图所示,下列实验操作与方法正确的是7.在K2SO4和Fe2(SO4)3的混合溶液中,已知Fe3+的物质的量浓度为0.1mol/L,而SO42—的物质的量浓度为0.3mol/L,则混合液中K+的物质的量浓度为()A.0.15mol/LB.0.3mol/LC.0.45mol/LD.0.6mol/L8.实验室用固体烧碱配制500mL0.1000mol/L的NaOH溶液。需称量________g烧碱,应放在________(填仪器名称)中称量.配制过程中,不需要的仪器(填写代号)_________A、烧杯B、量筒C、玻璃棒D、1000mL容量瓶E、漏斗F、胶头滴管G、500mL试剂瓶根据实验需要和(2)所列仪器判断,完成实验还缺少的仪器是_____________在容量瓶中确定溶液体积的过程中,最后加入少量水的做法是___________________9.配制100mL、1.0mol·L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是()A.容量瓶使用前经蒸馏水清洗后没有干燥B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒C.俯视确定凹液面与刻度线相切D.用敞口容器称量NaOH且时间过长10.原子结构模型的演变图中,⑴为道尔顿实心球式原子模型、⑵为卢瑟福行星运转式原子模型、⑶为汤姆生葡萄干面包式原子模型、⑷为近代量子力学原子模型、⑸为玻尔轨道式原子模型。其中符合历史演变顺序的一组排列是⑴⑵⑶⑷⑸A.⑴⑶⑵⑸⑷B.⑴⑵⑶⑷⑸C.⑴⑸⑶⑵⑷D.⑴⑶⑸⑷⑵11.Se是人体必需微量元素,下列关于说法正确的是()A.互为同素异形体B.互为同位素C.分别含有44和46个质子D.都含有34个中子12.已知自然界中铱有两种质量数分别为191和193的同位素,而铱的平均相对原子质量为192.22,这两种同位素的原子个数比应为A.39∶61B.61∶39C.1∶1D.39∶11