如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
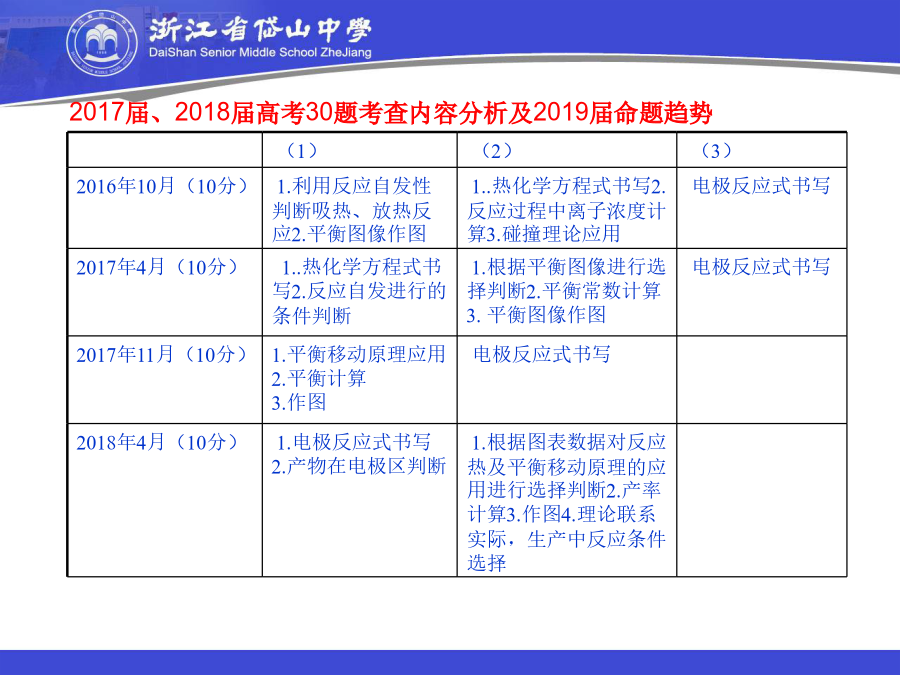
回顾2017届、2018届化学选考30题【2016.10】30.(10分)氯及其化合物在生活和生产中应用广泛。(1)已知:900K时,4HCl(g)+O2(g)③有研究表明,生成NaClO3的反应分两步进行:I2ClO—=ClO2—+Cl—IIClO2—+ClO—=ClO3—+Cl—常温下,反应II能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:______________________________________。(3)电解NaClO3水溶液可制备NaClO4。在电解过程中由于阴极上吸附氢气,会使电解电压升高,电解效率下降。为抑制氢气的产生,可选择合适的物质(不引入杂质),写出该电解的总化学方程式________________________________________。【2017.4】30.【加试题】(10分)以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。请回答:(1)已知:2Al2O3(s)===4Al(g)+3O2(g)ΔH1=3351kJ·molˉ12C(s)+O2(g)===2CO(g)ΔH2=-221kJ·molˉ12Al(g)+N2(g)===2AlN(s)ΔH3=-318kJ·molˉ1碳热还原Al2O3合成AlN的总热化学方程式是_______,该反应自发进行的条件__。(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4,总物质的量amol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。反应ⅠCO2(g)+4H2(g)CH4(g)+2H2O(g)ΔH4①下列说法不正确的是________A.ΔH4小于零B.温度可影响产物的选择性C.CO2平衡转化率随温度升高先增大后减少D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应Ⅰ的平衡常数为________(用a、V表示)③350℃下CH4物质的量随时间的变化曲线如图3所示。画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。【2017.11】30.(10分)(一)十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C10H18)→四氢萘(C10H12)→萘(C10H8)”的脱氢过程释放氢气。已知:C10H18(l)→C10H12(l)+3H2(g)ΔH1C10H12(l)→C10H8(l)+2H2(g)ΔH2ΔH1>ΔH2>0;C10H18→C10H12的活化能为Ea1,C10H12→C10H8的活化能为Ea2;十氢萘的常压沸点为192℃;在192℃,液态十氢萘脱氢反应的平衡转化率约为9%。请回答:(1)有利于提高上述反应平衡转化率的条件是________。A.高温高压B.低温低压C.高温低压D.低温高压(2)研究表明,将适量十氢萘置于恒容密闭反应器中,升高温度带来高压,该条件下也可显著释氢,理由是________。(3)温度335℃,在恒容密闭反应器中进行高压液态十氢萘(1.00mol)催化脱氢实验,测得C10H12和C10H8的产率x1和x2(以物质的量分数计)随时间的变化关系,如下图所示。(8,0.374)【2018.4】30.【加试题】(10分)(一)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图1所示。(1)收集到(CH3)4NOH的区域是______(填a、b、c或d)。(2)写出电池总反应________。2017届、2018届高考30题考查内容分析及2019届命题趋势2019届高考化学30题选考命题趋势例如:30题第一块内容(铝、氮及其化合物知识)回顾2017届、2018届化学选考31题Cu屑(含Fe)装置改进后,向仪器A中缓慢滴加SOCl2时,需打开活塞______(填“a”、‘‘b”或“a和b”)。(5)为测定无水Cu(NO3)2产品的纯度,可用分光光度法。已知:4NH3·H2O+Cu2+==Cu(NH3)4H2O;Cu(NH3)对特定波长光的吸收程度(用吸光度A表示)与Cu2+在一定浓度范围内成正比。现测得Cu(NH3)的吸光度A与Cu2+标准溶液浓度关系如图2所示:【2017.4】31.(10分)ClO2是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO2固体,以便运输和贮存。过氧化氢法制备NaClO2固体的实验装置如图1所示。已知:2NaClO