如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
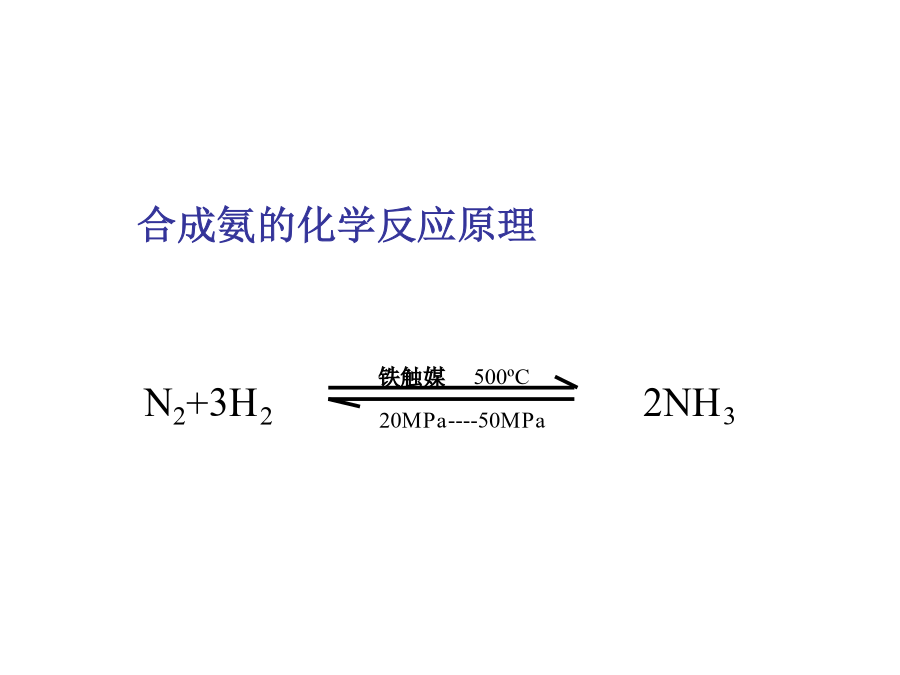
第四节合成氨条件的选择[问题2]要提高合成氨的生产效益,具体应从哪些方面来考虑?[讨论]根据外界条件对化学反应速率的影响,说明要使合成氨的化学反应速率增大,应采取哪些措施?应用化学平衡移动原理,说明要提高平衡混合物中氨气的含量,应采取哪些措施?请同学们对比下表的实验数据,检查自己的理论推断是否正确。分别从化学反应速率和化学平衡两个角度分析合成氨的合适条件。结论[讨论][讨论]使用催化剂:可以大大加快化学反应速率,提高生产效率,也提高了经济效益;合成氨工业的主要流程:[讨论]工业上选择适宜化工生产条件要坚持什么原则?参考题目:化学模拟生物固氮[小结]巩固练习2、在一密闭容器中,N2、H2合成氨的反应已达到平衡。此时再往容器中通入一定量N2,保持温度和容器体积不变,当反应再次达到平衡时,与第一次平衡状态相比()(A)NH3的百分含量增大(B)NH3的浓度增大(C)H2的转化率提高(D)N2的转化率提高3、在合成氨工业中,为增加NH3的日产量,下列变化过程不能使平衡向右移动的是()(A)不断将NH3分离出来(B)使用催化剂(C)采用500℃左右的高温(D)采用20MPa----50MPa的压强4、在合成氨时,可以提高H2转化率的措施是(A)延长反应时间(B)充入过量H2(C)充入过量N2(D)升高温度5、关于氨的合成工业的下列说法正确的是(A)从合成塔出来的气体,其中氨一般占15%,所以生产氨的工业的效率都很低(B)由于NH3易液化,N2、H2可循环使用,则总的说来氨的产率很高(C)合成氨工业的反应温度控制在500℃左右,目的是使平衡向正反应方向进行(D)合成氨工业采用20MPa----50MPa,是因该条件下催化剂的活性最好6、在一定条件下,将N2和H2的混和气体通入固定容积的密闭容器中进行合成氨反应:N2+3H22NH3(正反应为放热反应)下列图像表示正确的是:()7.下列反应达到平衡时,哪种条件下生成物的含量最高:X2(g)+2Y2(g)X2Y4(g)(正反应为放热反应)()A.高温高压B.低温低压C.高温低压D.高压低温8.对于反应:2SO2(g)+O2(g)2SO3(g)下列判断正确的是()A.2体积SO2和足量O2反应,必定生成2体积SO3B.其他条件不变,增大压强,平衡向右移动C.平衡时,SO2消耗速率必定等于O2的生成速率的两倍D.平衡时,SO2浓度必定等于O2浓度的两倍.9.在一定条件下,合成氨反应达到平衡后,混合气体中NH3的体积占25%,若反应前后条件保持不变,则反应后缩小的气体体积与原反应物体积的之比是()ABCD