如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
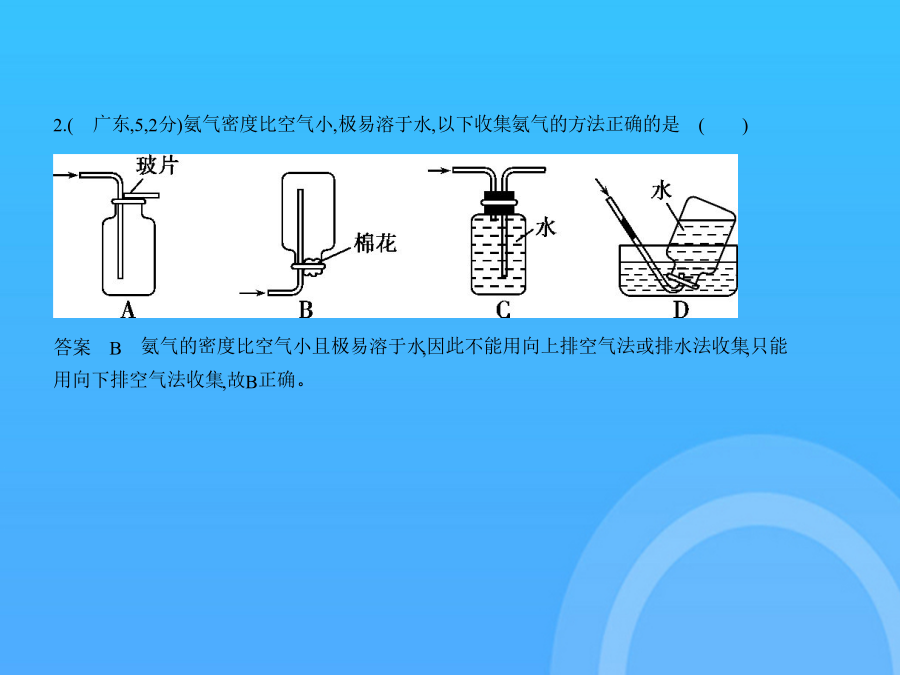
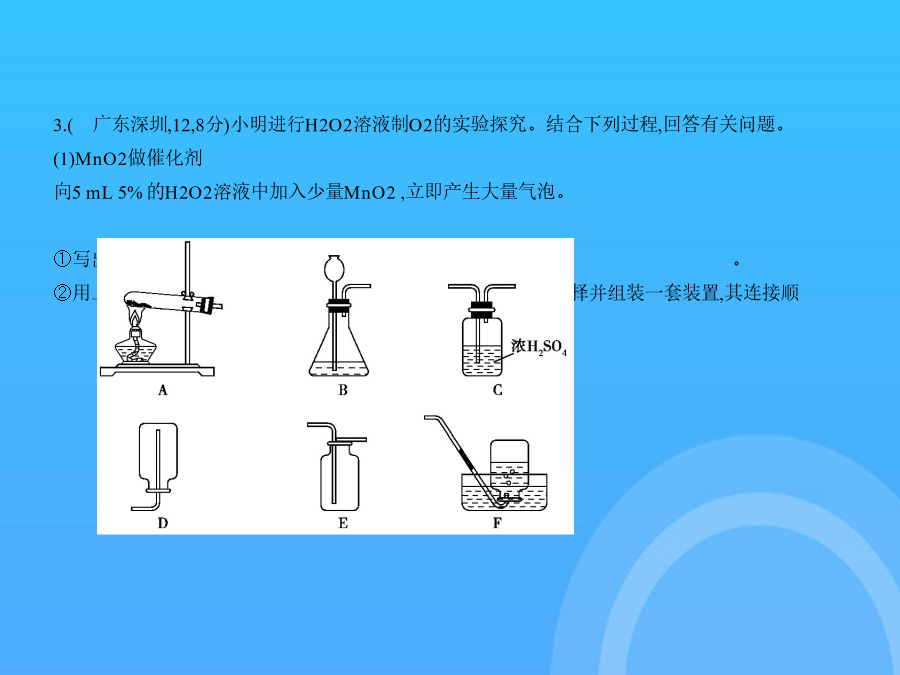
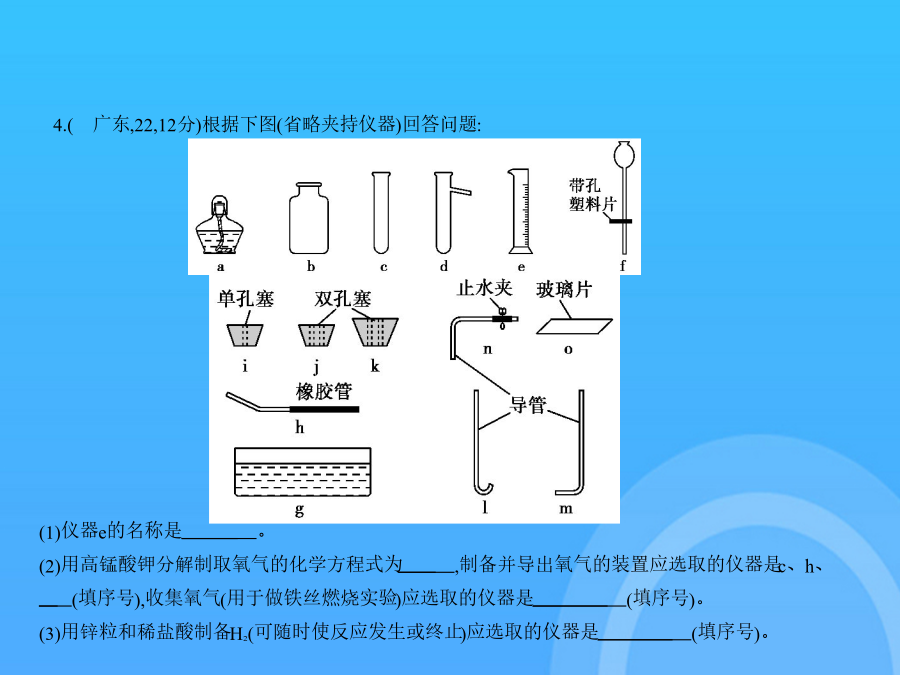
专题十三常见气体的制取与净化试题部分pptxA组—年广东中考题组考点1常见气体的制备2.(广东,5,2分)氨气密度比空气小,极易溶于水,以下收集氨气的方法正确的是 () 3.(广东深圳,12,8分)小明进行H2O2溶液制O2的实验探究。结合下列过程,回答有关问题。(1)MnO2做催化剂向5mL5%的H2O2溶液中加入少量MnO2,立即产生大量气泡。 ①写出用H2O2溶液制备O2的化学方程式:。②用上述反应原理制备并收集一瓶干燥的O2,从所给装置图中选择并组装一套装置,其连接顺序为→→(填标号)。为了确保实验成功,在装药品之前应该。③检验O2的方法是,若木条复燃,则证明收集的气体为O2。(2)FeCl3溶液做催化剂向5mL5%的H2O2溶液中加入2滴一定浓度的FeCl3溶液,立即产生大量气泡。【已知】FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-【问题】哪种微粒对H2O2溶液的分解起催化作用?【假设】假设一:可能是H2O假设二:可能是Fe3+假设三:可能是Cl-【分析】①假设一不可能成立,理由是。【实验】【结论】②假设成立,而假设一和另一种假设不成立。(3)催化剂比较从循环利用的角度分析,(填化学式)更适合做该反应的催化剂。4.(广东,22,12分)根据下图(省略夹持仪器)回答问题: (4)氢化钙(CaH2)常温下能与水反应生成H2,是野外工作人员便携燃料的来源。课外小组同学利用(3)中产生的H2与金属钙反应制取CaH2(见下图)。 答案(1)量筒(2)2KMnO4 K2MnO4+MnO2+O2↑a、ib、g、l或b、m、o(3)c、f、j、n或d、f、i、n(若选b,终止反应时液体不能全部进入f)(4)①ⅡⅢ②通入氢气把装置中的空气排尽③CaH2+2H2O 2H2↑+Ca(OH)2装浓H2SO4的洗气瓶解析(1)仪器e的名称为量筒。(2)高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO4 K2MnO4+MnO2+O2↑;使用高锰酸钾制备并导出氧气的装置即固体加热制取气体的装置,应选取的仪器是酒精灯、试管、导管、单孔橡胶塞,故选c、h、a、i;收集氧气(用于做铁丝燃烧实验)有两种方法:排水法和向上排空气法,对应的装置分别为“b、g、l”和“b、m、o”。(3)用锌粒和稀盐酸制备H2(可随时使反应发生或终止)的装置是固液不加热装置,若选用普通试管做反应发生器,可选仪器为c、f、j、n;若选用具支试管做反应发生器,可选仪器为d、f、i、n。(4)①制取氢气过程中容易混有氯化氢气体,应用氢氧化钠溶液除去,然后用浓硫酸除去其中的水蒸气,故m为氢氧化钠溶液,n为浓硫酸;②为防止钙被氧化,在加热钙之前必须进行的操作是先通一段时间氢气,排尽装置内的空气;③氢化钙与水反应生成氢气和氢氧化钙,反应的化学方程式为CaH2+2H2O 2H2↑+Ca(OH)2;为防止空气中的O2、CO2、水蒸气与玻璃管中Ca或CaH2反应,必须在导管末端再连接的装置是装浓H2SO4的洗气瓶。关键点拨第(4)①题中,气体净化时,先除去杂质气体,再干燥气体,故先将气体通过氢氧化钠溶液,再通过浓硫酸。5.(广东广州,27,8分)下图是实验室制备气体的部分装置。 (1)加热混有二氧化锰的氯酸钾制备一瓶氧气用于性质实验。①该方法制得O2的化学方程式是。②可选用与(填序号)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后,观察到有气泡冒出,说明装置气密性良好。(2)氢气被认为是理想的清洁、高能燃料。①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用(填序号)与E装置组合,在E导管口点燃。实验过程是:组装仪器→检查装置气密性→装入药品制备氢气→→点燃。②电解水也可制得H2。装置如图F,管中产生的是氢气。③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是。A.用矿石生产锌和硫酸,再相互反应B.在催化剂作用下,利用太阳能光解水C.利用煤燃烧发电,再电解水D.利用风能、水力发电,再电解水答案(1)①2KClO3 2KCl+3O2↑②BC双手握住试管(2)①A验纯②甲③BD6.(广东,22,12分)根据下图回答有关问题。 答案(12分)(1)漏斗(1分)C(1分)2KClO3 2KCl+3O2↑(2分)(2)塑料片上(1分)c(1分)向长颈漏斗中加入一定量水(1分),若水面下降到一定程度后能稳定保持液面不再下降(1分)(3)B(1分)固液不能分离(或不能把液体压入长颈漏斗,1分)(4)B(1分)b(1分)解析(1)仪器a的名称是漏斗;因反应物KC