如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
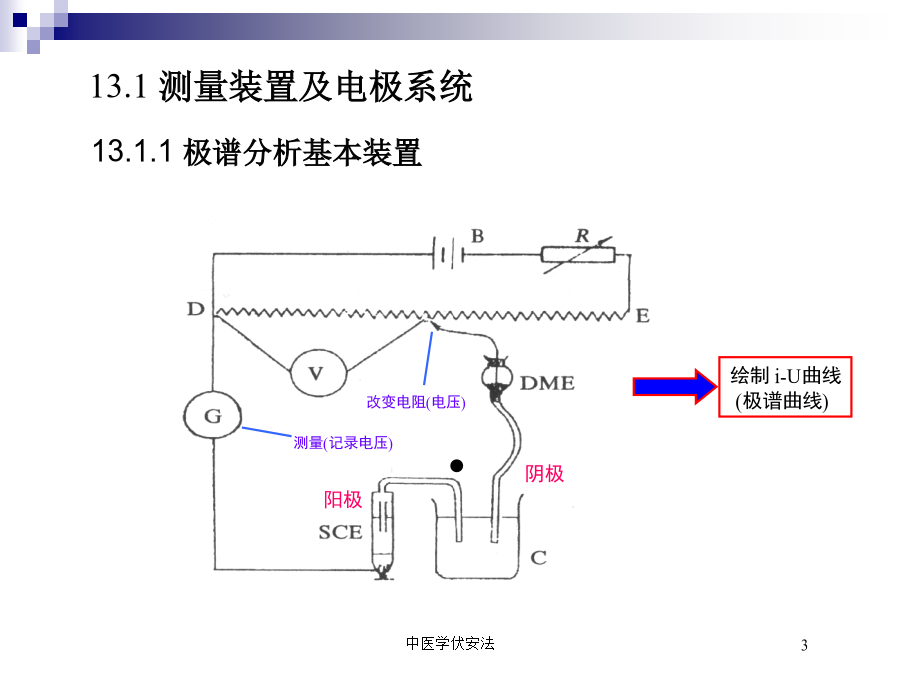
中医学伏安法定义:伏安法和极谱法是一种特殊的电解方法。以小面积、易极化的电极作工作电极,以大面积、不易极化的电极为参比电极组成电解池,电解被分析物质的稀溶液,由所测得的电流-电压特性曲线来进行定性和定量分析的方法。当以滴汞作工作电极时的伏安法,称为极谱法,它是伏安法的特例。13.1测量装置及电极系统三电极系统及装置:实际工作中,当回路电流较大或内阻较高时,此时参比电极也发生极化,并产生iR降。此时测得的是i~V曲线,而不是i-曲线!此时半波电位负移,总电解电流减小且极谱波变形。此时要准确测定滴汞电极电位,必须克服iR降!通常的做法是使用三电极系统,如下图所示。极谱电流i容易从回路WC中测得,滴汞工作电极电位可由高阻抗回路WR中获得(因阻抗高,因而此回路无明显电流通过),即可通过此监测回路显示。伏安法的工作电极汞电极:挤压式悬汞电极、挂吊式悬汞电极、汞膜电极(以石墨电极为基质,在其表面上镀上一层汞得到)。其它固体电极:玻碳电极、铂电极和金电极等。汞电极不适合在较正电位下工作,而固体电极则可以。13.2极谱曲线电压由0V逐渐增加到-1.2V左右,绘制电流-电压曲线。图中①~②段,仅有微小的电流流过,这时的电流称为“残余电流”或背景电流。当外加电压到达Pb2+的析出电位时,Pb2+开始在滴汞电极上迅速反应。这就是极谱分析的定量分析基础。注意:式中极限电流id包括残余电流iR(不由扩散产生),故极限电流减去残余电流即为极限扩散电流。当电流等于极限扩散电流的一半时所对应的电位称之为半波电位(E1/2),由于不同物质其半波电位不同,因此半波电位可作为极谱定性分析的依据。极谱分析的特点:(一)参比电极——在极谱分析中电流是很小的,而参比电极的面积较大,所以电流密度很小,[Cl-]的改变也很小。(二)滴汞电极:1.电极电位完全受外加电压的控制2.由于滴汞电极的面积很小,所以,极谱分析中微小的电流在滴汞电极上也要产生很大的电流密度。3.滴汞和周围的溶液始终保持新鲜──保证同一外加电压下的电流的重现和前后电解不相互影响。4.汞电极对氢的超电位比较大──可在酸性介质中进行分析(对SCE,其电位可负至-1.2V)。5.滴汞作阳极时,因汞会被氧化,故其电位不能超过+0.4V。即该方法不适于阴离子的测定。6.汞易纯化,但有毒,易堵塞毛细管。13.2.2极谱定量分析基础一、定量公式:极限扩散电流平均极限扩散电流尤考维奇(Ilkoviĉ)公式。其中id—极限扩散电流(A)—平均极限扩散电流(A);z—电子转移数D—扩散系数(cm2/s);m—汞滴流量(g/s);t—测量时,汞滴周期时间(s);c—待测物浓度(mmol/L)。二、影响扩散电流的因素a)溶液组份的影响组份不同,溶液粘度不同,因而扩散系数D不同。分析时应使标准液与待测液组份基本一致——底液。b)毛细管特性的影响汞滴流速m、滴汞周期t是毛细管的特性,将影响平均扩散电流大小。通常将m2/3t1/6称为毛细管特性常数。设汞柱高度为h,因m=k’h,t=k’’/h,则毛细管特性常数m2/3t1/6=kh1/2,即与h1/2成正比。因此,实验中汞柱高度必须一致。该条件常用于验证极谱波是否扩散波。c)温度影响除z外,温度影响公式中的各项,尤其是扩散系数D。室温下,温度每增加1oC,扩散电流增加约1.3%,故控温精度须在0.5oC。三、干扰电流极其消除除扩散电流外,极谱电流还包括:残余电流;迁移电流;极谱极大;氧波。这些电流应设法扣除!2.迁移电流(Migrationcurrent)产生:由于电极对待测离子的静电引力导致更多离子移向电极表面,并在电极上还原而产生的电流,称为迁移电流。它不是因为由于浓度陡度引起的扩散,与待测物浓度无定量关系,故应设法消除。消除:通常是加入支持电解质(或称惰性电解质)——类似于缓冲液。3.极谱极大(Maximumcurrent)产生:当外加电压达到待测物分解电压后,在极谱曲线上出现的比极限扩散电流大得多的不正常的电流峰,称为极谱极大。消除:加入可使表面张力均匀化的极大抑制剂,通常是一些表面活性物质如明胶、PVA、TritonX-100等。4.氧波(Oxygenwaves)产生:两个氧极谱波:O2+2H++2e=H2O2-0.2V(半波电位)H2O2+2H++2e=2H2O-0.8V(半波电位)消除:a)通入惰性气体如H2、N2、CO2(CO2仅适于酸性溶液);b)在中性或碱性条件下加入Na2SO3,还原O2;c)在强酸性溶液中加入Na2CO3,放出大量二氧化碳以除去O2;或加入还原剂如铁粉,使与酸作用生成H2,而除去O2;d)在弱酸性或碱性溶液中加入抗坏