如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
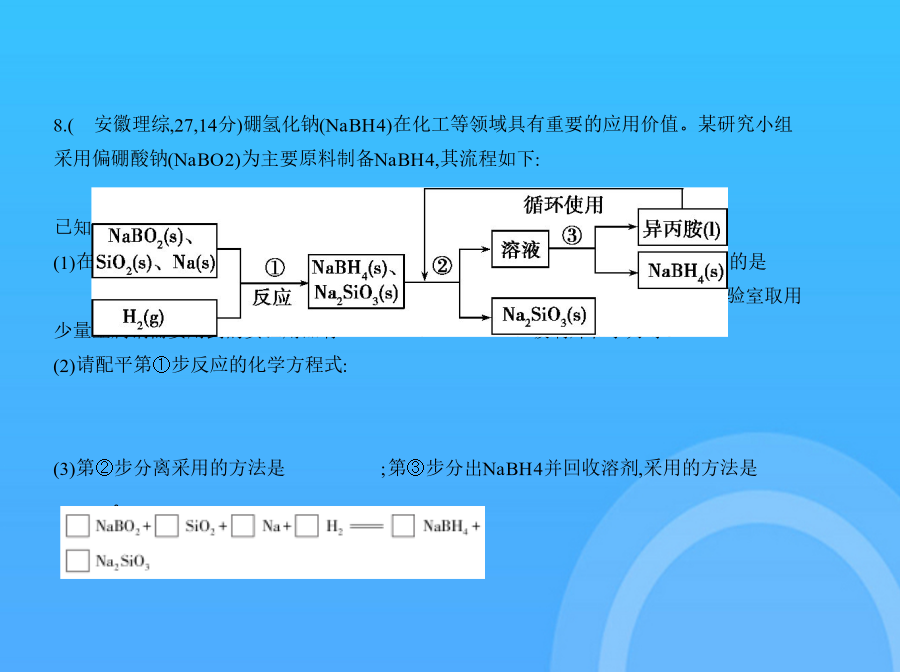
专题十二钠铝及其化合物考点一钠及其化合物A组自主命题·北京卷题组1.(北京理综,7,6分)下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是 ()2.(北京理综,7,6分)下列解释实验现象的反应方程式正确的是 ()A.切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2 Na2O22S溶液,白色沉淀变成黑色2AgCl+S2- Ag2S↓+2Cl-2O2在潮湿的空气中放置一段时间,变成白色黏稠物2Na2O2+2CO2 2Na2CO3+O23溶液中加入过量的澄清石灰水,出现白色沉淀2HC +Ca2++2OH- CaCO3↓+C +2H2O3.(江苏单科,9,2分)在给定条件下,下列选项所示的物质间转化均能实现的是 ()3(s) Na2CO3(s) NaOH(aq)B.Al(s) NaAlO2(aq) Al(OH)3(s)3(aq) [Ag(NH3)2]+(aq) Ag(s)2O3(s) Fe(s) FeCl3(aq)4.(课标Ⅱ,7,6分)化学与生活密切相关。下列说法错误的是 ()5.(江苏单科,3,2分)下列有关物质性质与用途具有对应关系的是 ()2O2吸收CO2产生O2,可用作呼吸面具供氧剂2具有还原性,可用于自来水的杀菌消毒2硬度大,可用于制造光导纤维3易溶于水,可用作制冷剂6.(山东理综,10,5分)某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是 ()32227.(福建理综,6,6分)下列有关物质应用的说法正确的是()8.(安徽理综,27,14分)硼氢化钠(NaBH4)在化工等领域具有重要的应用价值。某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下: 已知:NaBH4常温下能与水反应,可溶于异丙胺(沸点:33℃)。(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是。原料中的金属钠通常保存在中,实验室取用少量金属钠需要用到的实验用品有、、玻璃片和小刀等。(2)请配平第①步反应的化学方程式:(3)第②步分离采用的方法是;第③步分出NaBH4并回收溶剂,采用的方法是。(4)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是。解析(1)原料中的Na及H2会与空气中的O2反应,原料中的Na及产物NaBH4会与水反应,故第①步反应加料之前应先将反应器加热至100℃以上并通入氩气,以除去反应器中的空气和水蒸气。(2)运用化合价升降法和观察法,不难配平所给反应的化学方程式。(3)由题给信息可知,欲分离NaBH4和异丙胺可加热蒸馏,馏分为异丙胺,留在蒸馏烧瓶中的是NaBH4固体产品。(4)依题意可知,反应NaBH4(s)+2H2O(l) NaBO2(s)+4H2(g)的ΔH=-21.6kJ÷ =-216.0kJ·mol-1。9.(浙江理综,27-Ⅱ,12分)化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。请推测并回答:(1)甲的化学式。(2)甲与AlCl3反应得到NaAlH4的化学方程式。(3)NaAlH4与水发生氧化还原反应的化学方程式。(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式。(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到的固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。判断该同学设想的制备和验纯方法的合理性并说明理由。解析(1)4.80g甲中氢元素的质量为 ×2×1g·mol-1=0.2g,则钠元素的质量为4.80g-0.2g=4.60g,n(Na)∶n(H)= ∶ =1∶1,所以甲的化学式为NaH。(2)甲与AlCl3反应得到NaAlH4的化学方程式为4NaH+AlCl3 NaAlH4+3NaCl。(3)NaAlH4与水发生氧化还原反应的化学方程式为NaAlH4+2H2O 4H2↑+NaAlO2。(4)根据题意可知,甲在无水条件下能将铁锈中的铁还原为铁单质,化学方程式为3NaH+Fe2O3 2Fe+3NaOH。(5)制备过程和验纯方法均不合理。制备过程中所用的盐酸易挥发,H2中混有HCl,会导致产物中混有NaCl,故不合理。若与钠反应的H2不足,固体产物中会有Na残留,残